El modelo atómico de Bohr o de Bohr-Rutherford es un modelo clásico del átomo, pero fue el primer modelo atómico en el que se introduce una cuantización a partir de ciertos postulados (ver abajo). Fue propuesto en 1913 por el físico danés Niels Bohr, para explicar cómo los electrones pueden tener órbitas estables alrededor del núcleo y por qué los átomos presentaban espectros de emisión característicos (dos problemas que eran ignorados en el modelo previo de Rutherford). Además el modelo de Bohr incorporaba ideas tomadas del efecto fotoeléctrico, explicado por Albert Einstein en 1905.
Postulados de Bohr
En1913, Niels Bohr desarrolló su célebre modelo atómico de acuerdo a tres postulados fundamentales.
Primer postulado
Los electrones describen órbitas circulares en torno al núcleo del átomo sin radiar energía.
La causa de que el electrón no radie energía en su órbita es, de momento, un postulado, ya que según la electrodinámica clásica un carga en movimiento acelerado debe emitir energía en forma de radiación.
Para conseguir el equilibrio en la órbita circular, las dos fuerzas que siente el electrón: la fuerza coulombiana, atractiva, por la presencia del núcleo y la fuerza centrífuga, repulsiva por tratarse de un sistema no inercual, deben ser iguales en módulo en toda la órbita. Esto nos da la siguiente expresión:
- Donde el primer término es la fuerza eléctrica o de Coulomb, y el segundo es la fuerza centrífuga; k es la constante de la fuerza de Coulomb, Z es el número atómico del átomo, e es la carga del electrón, me es la masa del electrón, v es la velocidad del electrón en la órbita y r el radio de la órbita.
Segundo postulado
No todas las órbitas para electrón están permitidas, tan solo se puede encontrar en órbitas cuyo radio cumpla que el momento angular, L, del electrón sea un múltiplo entero de h' = h / 2 π
. Esta condición matemáticamente se escribe:
- con n = 1, 2, 3, ...
A partir de ésta condición y de la expresión para el radio obtenida antes, podemos eliminar v y queda la condición de cuantización para los radios permitidos:
- con n = 1, 2, 3, ...
- subíndice introducido en esta expresión para resaltar que el radio ahora es una magnitud discreta, a diferencia de lo que decía el primer postulado.
Ahora, dándole valores a n, número cuántico principal, obtenemos los radios de las órbitas permitidas. Al primero de ellos (con n=1), se le llama radio de Bohr.:
- expresando el resultado en angstrom.
Tercer postulado
El electrón solo emite o absorbe energía en los saltos de una órbita permitida a otra. En dicho cambio emite o absorbe un fotón cuya energía es la diferencia de energía entre ambos niveles. Este fotón, según la ley de Planck tiene una energía:
- donde ni identifica la órbita inicial y nf la final, y ν es la frecuencia.

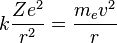
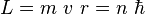



me gusto mucho toda esta pagina
ResponderBorrarMe gusto y me aydo muchas gracias:)
ResponderBorrarbueno tengo trabajo de ciencias y esta pagina me ayudooooooo gracias :)
ResponderBorrarEstas formulas son bellisimas<3 las ame<3
ResponderBorrar